問 題
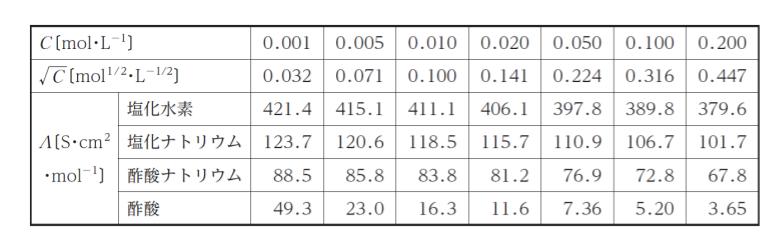
表は、塩化水素、塩化ナトリウム、酢酸ナトリウム、酢酸の水溶液濃度 C〔mol・L-1〕とモル伝導度 K〔S・cm2・mol-1〕の関係を表したものである。この値から、酢酸の無限希釈のモル伝導度及び濃度 0.01 mol・L-1 の水溶液における酢酸の解離度を求める。これらの組合せとして最も妥当なのはどれか。ただし、必要ならば方眼を用いよ。
正解.5
解 説
強電解質で、横軸に√c 、縦軸にΛを取ると、直線関係となります。これをコールラウシュの法則と呼びます。弱電解質では、急激に減少します。
方眼紙を使わなくてもいいと思うのですが、√C = 0.100 → 0.071 → 0.032 という順番に見れば、酢酸の Λ が 16.3 → 23.0 → 49.3 と急激な上昇を見せているのがわかると思います。この勢いからすれば、選択肢から 91 では終わらないだろうと考えられます。正解は 4 or 5 です。
解離度(電離度) α は、モル伝導率 Λ と極限モル伝導率 Λ0 の比で表されます。濃度 0.01 mol/L の時の酢酸の Λ は、表より 16.3 です。従って 16.3/391 ≒ 4/100 です。選択肢より選ぶと 4.2 % です。
以上より、正解は 5 です。
参考 物理化学 3-2-4
類題 97-93

コメント