問 題
ベンゼンの6員環の六つの炭素原子について、ある炭素原子を炭素1とし、時計回りに炭素2、 炭素3、 … 炭素6とする。φk を k に対応する番号の炭素原子の 2pz 原子軌道(z はベン
ゼン環を含む平面に垂直な座標軸)とすると、ベンゼンの6員環に非局在化した分子軌道の波動
関数 Ψn (n = 1~ 6) は、ヒュッケル近似のもとで、次のように表すことができる。このとき、Ψ2 と同じエネルギーをもつ分子軌道の波動関数はどれか。
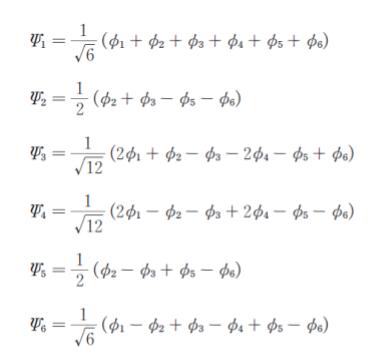
1. Ψ1
2. Ψ3
3. Ψ4
4. Ψ5
5. Ψ6
解 説
「分子軌道の波動関数」は、「構成原子の原子軌道を表す波動関数」の「線形結合(ax+by+・・・の形)」で表すことができます。Π 分子軌道の波動関数 Ψ = c1φ+c2φ+c3φ+c4φ+c5φ+c6φ とおけるということです。 符号が「+」なのか「ー」なのかだけに注目すると、まず Ψ1 は以下のように表すことができます。
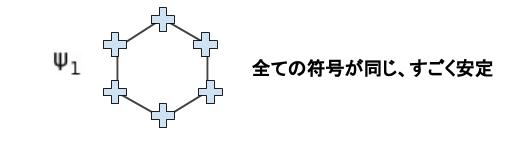
※軌道の符号が同じ同士がとなりあうと「結合性分子軌道」で「安定」と読みます。符号が逆は「反結合性分子軌道」で「不安定」と読みます。
Ψ2 ~ Ψ6 を同様に表すと以下のようになります。
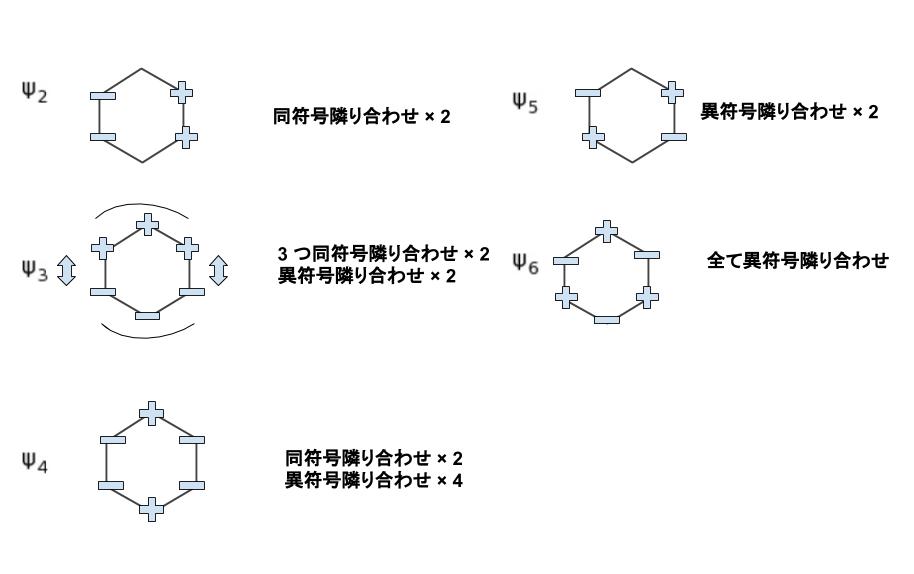
Ψ2 と同じエネルギー、つまり「同符号隣り合わせ × 2」ぐらい安定と思われるのは、Ψ3 です。
以上より、正解は 2 です。
(ちなみに、Ψ4 と Ψ5 も同じエネルギーだろうと読み取れます。)
ーーー
2026.03.05 追記:別の考え方
分子軌道の波動関数において、エネルギーの高さ(安定性)は、軌道の符号(位相)が逆転する箇所の数、すなわち「節の数」によって比較することができます。 波の性質上、節の数が多いほど反結合性が強くなり、エネルギーが高く(不安定に)なります。
各波動関数(Ψ1~Ψ6)について、符号が逆転している箇所(節の数)を数えると、以下のようになります。
Ψ1:節の数 0 (最も安定)
Ψ2:節の数 2
Ψ3:節の数 2
Ψ4:節の数 4
Ψ5:節の数 4
Ψ6:節の数 6 (最も不安定)
この結果から、Ψ2 と Ψ3 は節の数が共に「2」で等しいため、同じエネルギーを持つことが予測できます。
以上より、正解は 2 です。

コメント
はじめまして、いつもこちらのサイトを役立たせていただいております。
この問題ですが、「位相が逆になる際の節」が多い方が分子軌道が不安定化することを用いれば、定量的に示せるのではないかと思います。
具体的には、節の数が
Ψ1:0 2:2 3:2 4:4 5:4 6:6
となるので、節の数がΨ2と等しいΨ3が同じエネルギーを持つと予測できます
https://kusuri-jouhou.com/chemistry/homo.html
こちらのサイト等を参考にしました。
今後もこちらを活用させていただきます。
コメントありがとうございます!
別の考え方として追記して解説を修正いたしました。
引き続き活用していただければ幸いです!