この項では、炭素に直接結合している水素の酸性度の比較について考えます。
炭化水素の酸性度
まずは単純な構造のものとして、アルカン、アルケン、アルキンの比較から入ります。
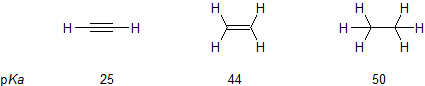
アセチレン、エチレン、エタンのpKa は上図の通りとなります。これは、sp3混成軌道よりもsp2混成軌道のほうが、sp2混成軌道よりもsp混成軌道のほうが酸性度が大きいことを示しています。
つまり酸性度の大きさは、s性が関係しています。sp混成軌道はs性が50%ありますが、sp2混成軌道はs性が33%、sp3混成軌道はs性が25%しかありません。
s性が高いほど電子は原子核の近くにあるということになり、その分負電荷を安定化させやすいので、H+を放出して陰イオンになりやすい(=酸となりやすい)といえます。
置換基による酸性度の比較
炭素酸の酸性度は、その水素に付く炭素の隣にどのような置換基があるかで大きく変わってきます。例えばニトロ基が付くと酸性度がかなり高くなり、フェニル基が付くと少しだけ高くなる、といった具合です。
ここでも炭化水素のときと同様、H+を放出して陰イオンになりやすいかどうかで酸性度の大小が決まります。
各置換基による酸性度の大きさは、以下の通りです。ニトロ基が最も酸性度が高く、アルキル基が低くなります。縦に並べてあるもの(エステルとシアンなど)は大体同じくらいと考えてください。
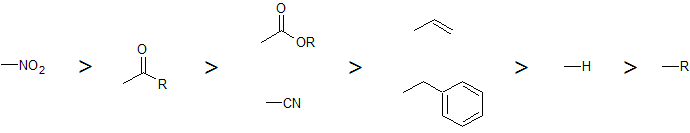

コメント