フェノール類の性質
アルコール類は、有する-OH 基の数によって一価、二価、三価と呼んでいましたが、フェノール類でも同様です。
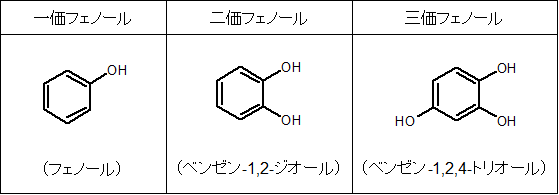
また、アルコール類は中性でしたが、フェノール類は酸性を示します。その理由は、フェノールからプロトンが抜けたフェノキシドイオンが以下のような共鳴により安定化するためです。
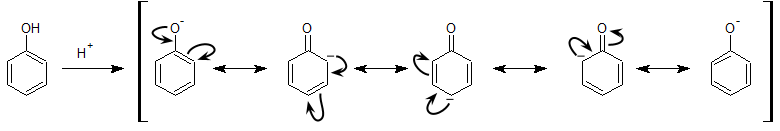
フェノール類の反応
フェノール類の代表的な反応として、以下の5つを紹介します。
- エーテルへの変換(Williamson エーテル合成)
- ベンゼン環の o,p 位での求電子置換反応
- 多価フェノール類の酸化反応
- Fe3+ を用いた呈色反応
- Gibbs 反応
1 つ目はフェノール類のエーテルへの変換です。
これはアルコール類の反応(前項参照)で示した Williamson (ウィリアムソン)エーテル合成と同じです。つまり、1 段階目で塩基によるプロトンの引き抜きが起こります。次いで 2 段階目でハロアルカンとの SN2反応が起こって、エーテルを生成します。
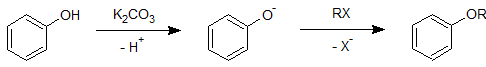
2 つ目はベンゼン環の o,p 位での求電子置換反応です。最初に以下の反応例を見てください。
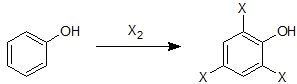
フェノール類に求核試薬を反応させると、求電子置換反応が起こります。フェノール類は o,p 配向性を示し、かつ強い電子供与性を持つため、一置換体ではなく上記の例のように複数の箇所で置換することが多いです。
配向性については反応性・配向性に及ぼす置換基の効果のページを参照してください。
3 つ目は多価フェノール類の酸化反応です。
最も単純な多価フェノールは、二価のヒドロキノンです。これに酸化剤(過ヨウ素酸ナトリウムや二クロム酸ナトリウムなど)を反応させると、酸化されてキノンが生成します。キノンと還元剤を用いることで逆反応も起こり、ヒドロキノンとなります。

4 つ目は Fe3+ を用いた呈色反応です。この反応は、ある化合物がフェノール性水酸基を有するかどうかを調べる定性試験として利用されます。
フェノール類に塩化鉄(Ⅲ)(FeCl3)を反応させると、錯体形成により紫系の色を呈色します。基質の構造の違いで呈色する色は青、青紫、紫、赤紫など差はありますが、フェノール類でなければ呈色しません。
5 つ目は Gibbs (ギブス)反応で、これも呈色を利用した定性試験に用いられます。
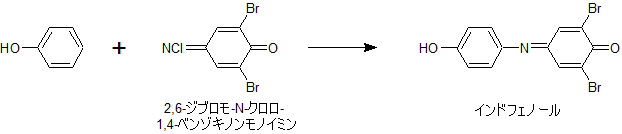
2,6-ジブロモ-N-クロロ-1,4-ベンゾキノンモノイミンという試薬がフェノール類と反応すると、インドフェノール類が生成し、呈色を示します。
試薬、生成物の構造は以下の反応式で確認してください。

コメント