前項まででたびたび乳酸の例を出しましたが、2つの異性体を「R-乳酸」「S-乳酸」と呼んで区別していました。立体異性体は互いの分子構造は同じですが、その空間的な配置だけが違います。この空間的な配置のことを「絶対配置」といいます。
それぞれの立体異性体は別の物質であるため、絶対配置を正確に区別する必要がありますが、その表示方法はいくつかあります。絶対配置の表示法の代表的なものは、以下の4つです。
- RS表示
- DL表示
- cis-trans表示
- E-Z表示
RS表示
RS表示は、不斉炭素に結合する原子(原子団)の空間配列を示すために、もっとも良く使われる表示法です。そのため有機化学を学ぼうとする方なら、とある構造式を見せられた時にそれがR体なのかS体なのかを正確に判断できるようになる必要があります。
R体かS体かを判断するには、以下の手順に従ってください。
- 不斉炭素に結合した4つの原子(原子団)に①番~④番までの優先順位をつけます。
- 優先順位の最も低い④番の原子(原子団)を紙面奥側になるように構造式を回転させます。
- 残った優先順位①~③番の原子(原子団)を①→②→③になるように見た時、それが時計回 り(右回り)ならR体、反時計回り(左回り)ならS体です。
これがRS表示の全てですが、これだけでは非常にわかりづらいので、順を追ってくわしく説明します。まず、以下の図を見てください。
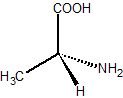
図1
図1の構造式を例に、上述の手順に従っていきます。まずは手順1.の通り、4つの原子(原子団)に優先順位を付けます。
この例では不斉炭素に直接結合している4つの原子は「C」「C」「H」「N」です。この中で原子番号の大きいものから順に優先順位が高くなります。よって、「N」が①番で、2つの「C」が②番と③番、「H」が④番となります。
ここで同じ原子だった2つの「C」ですが、原子団まで拡張して考えると「COOH」と「CH3」という違いが見えてきます。
不斉炭素と結合している炭素のさらに隣の原子を考えると、「COOH」は「O」であり、「CH3」は「H」であるため、より原子番号の大きい「O」を含む「COOH」のほうが優先順位が高いことになります。
よって、優先順位は①NH2、②COOH、③CH3、④H の順番になります。
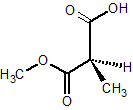
図2
少し脱線しますが、図2の構造式での優先順位がどうなるのかを考えてみてください。先に正解を示すと、①COOCH3、②COOH、③CH3、④Hです。
考え方としては、不斉炭素の隣についている原子は「C」が3つと「H」が1つです。この時点で「H」は原子番号が小さいため、順位が④番と決まります。
次に、不斉炭素の隣の「C」のさらに隣を考えますと、COOCH3が「O」、COOHも「O」、CH3は「H」となるため、CH3の順位が③番となります。
そして、不斉炭素の隣の「C」のさらに隣の「O」のまた隣を考えますと、COOCH3が「C」、COOHが「H」となりますので、COOCH3が①番、COOHが②番であると決まります。
さて、話を図1の化合物に戻します。
4つの原子(原子団)の優先順位が決まったため、手順2.にあるように、④番の原子(原子団)が紙面の奥側にくるように構造式を回転させます。
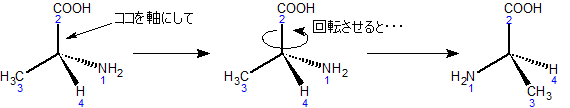
図3
図3のように、左の構造式の縦線で示した結合を軸にしてぐるっと廻すと、右の構造式になります。また、青色の数字は先ほど付けた優先順位です。手順2はこれで完了です。
手順3では、優先順位①~③番の原子(原子団)を①→②→③の順に見ていきます。
図3の右側の構造式で考えるので、①左下→②上→③右下になるかと思います。この順番で円を描くと時計回り(右回り)になることがわかります。この時、その化合物はR体であると決めることがきでるわけです。
もしも反時計回り(左回り)になれば、その化合物はS体です。
以上がRS表示を決める手順となります。
DL表示
DL表示は糖やアミノ酸においてよく用いられますが、DであるかLであるかを判断させられる場面はほとんどないと思います。そのため、エナンチオマーである2つの化合物の一方がD体であるなら、他方はL体である。というくらいを覚えておけば大丈夫です。
特に生化学において糖やアミノ酸を学ぶ際にはよく目にする表記かもしれませんが、やはり構造からDかLかを当てる必要はありません(私の知る限り)。
ひとつだけ注意しておいて欲しいことは、RS表示とDL表示はなんら関連性がないということです。とある化合物がRS表示でR体でありDL表示でD体だったからといって、他の化合物でもそうとは限りません。RS表示だとR体でDL表示だとL体であるという化合物も存在します。
cis-trans表示
cis-trans表示は高校の化学でも出てくるため、すでにご存知かもしれません。二重結合や環構造を持つ化合物に対して、置換基が同じ側にあればcis体(シス体)、反対側にあればtrans体(トランス体)となります。
cis-trans表示は二重結合につく置換基が同一置換基である場合に多く用いられます。もし置換基が違えば、一般的には下にあるE-Z表示を使います。
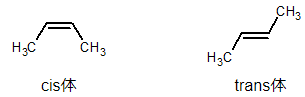
図4
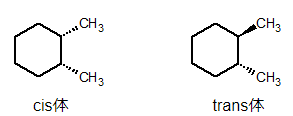
図5
E-Z表示
二重結合につく置換基は2×2=4つありますが、そのうちH以外の置換基が3つ以上あったりすると、cis-trans表示ではわかりにくくなってしまします。このような時に便利なのがこのE-Z表示です。
立体の決め方を説明するために、まずは下の構造を見てください。
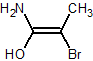
図6
実在するかどうかはともかく、図6のような化合物があるとします。立体を決めるために、まずは置換基に優先順位をつけます。
二重結合の左側にはNH2基とOH基がありますが、RS表示のところで学んだ優先順位の付け方をそのまま適用して、原子番号の大きいOH基が優先順位の高い置換基、NH2基が低い置換基となりました。
二重結合の右側でも同様に考えると、Br基が優先順位の高い置換基で、CH3基は低い置換基となります。
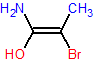
図7
以上の説明から、図7の赤色の置換基の優先順位が高く、青色の置換基の優先順位が低いことになります。この時、優先順位の高い置換基(赤色)同士が同じ側にあればZ配置、反対側にあればE配置となります。
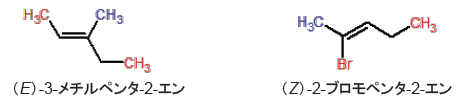
図8
以上が、主な絶対配置の表示法になります。

コメント