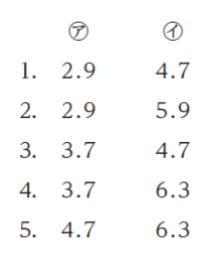
問 題
酢酸、酢酸ナトリウム及びそれらの混合液の pH に関する次の記述の ㋐、㋑ に当てはまるものの組合せとして最も妥当なのはどれか。ただし、酢酸の酸解離定数 Ka は、Ka = 1.8 × 10-5 mol・L-1 (pKa = 4.7) とする。
「0.10 mol・L-1 の酢酸水溶液の pH は、 ㋐である。一方、0.10 mol・L-1 の酢酸ナトリウム水溶液の pH は、8.9 である。0.10 mol・L-1 の酢酸水溶液と 0.10 mol・L-1 の酢酸ナトリウム水溶液を、同体積混合すると、その水溶液の pH は、 ㋑ となる。」
解 説
弱酸 HA の電離による pH、弱塩基 B の電離による pH、弱酸と強塩基から生じた塩の pH、強酸と弱塩基から生じた塩の pHの 4 パターンについては、公式を覚えて対応するのがよいと思われます。
・弱酸 HA の電離による pH→[H+]=√(Ka・C)
・弱塩基 B の電離による pH→[OH–]=√(Kb・C)なので、[H+]=Kw/√(Kb・C)
・弱酸と強塩基から生じた塩の pH→ 弱塩基による電離と同じ。
・強酸と弱塩基から生じた塩の pH→ 弱酸による電離と同じ。 となります。
※ 大前提となるのは Ka・Kb = Kw です。Kw とは、水のイオン積のことです。また、pH のように小文字の p を付けるのは「ーlog10」という意味です。
㋐ ですが
「弱酸 HA の電離による pH」のパターンです。公式に値を代入し、両辺 -log10 をとって計算します。以下のように計算をすすめると
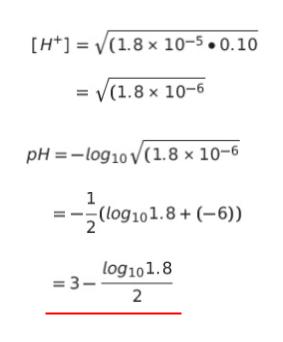
pH が 3 より小さいと評価できるので、選択肢より pH = 2.9 です。正解は 1 or 2 です。
㋑ ですが
酢酸と酢酸ナトリウム、つまり弱酸とその塩なので緩衝溶液です。ヘンダーソン・ハッセルバルヒの式を思い出します。pH = pKa + log[A– (イオン形)]/[HA (分子形)]…(1) です。
酢酸ナトリウムは完全に電離するので、イオン形が 0.1 mol/L です。酢酸はほぼ電離しないので、分子形を 0.1 mol/L とします。log1 = 0 なので (1) の log の項がなくなり「pH = pKa」 となります。つまり、pH = 4.7 です。
以上より、正解は 1 です。
類題 R1no4 弱塩基の pH
https://yaku-tik.com/yakugaku/km-r1-04/

コメント