問 題
ある反応は触媒 X 又は触媒 Y によって促進される。この反応の活性化エネルギーを 27 ℃ で測定したところ、触媒 X を用いた場合は 40 kJ・mol-1、触媒 Y を用いた場合は 55 kJ・mol-1 であった。このとき、触媒 X を用いた場合の反応速度定数 kX と触媒 Y を用いた場合の反応速度定数 kY の比 kX/kY はおよそいくらか。ただし、反応速度定数 k と活性化エネルギー Ea の間には
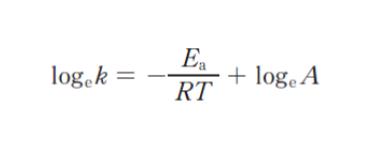
の関係が成り立つものとする。ここで、R は気体定数、T は絶対温度、A は頻度因子である。また、A は触媒 X を用いた場合と触媒 Y を用いた場合とで等しいものとし、R を 8.3 J・K-1・mol-1、自然対数の底 e を 2.7 とする。
1. 2.6 × 10-3
2. 1.0
3. 1.4
4. 3.9 × 102
5. 1.5 × 103
解 説
求めたいのが kX/kY です。log であれば log kX – log kY = log kX/kY になるので、まずはこの形を作ることを考えて式を操作していきます。
k に kX、Ea に 40000 を代入した式と
k に kY、Ea に 55000 を代入した式を並べて引きます。
※「k」を ×103 と数値になおしています。
※ 27℃ = 300 K になおしています。
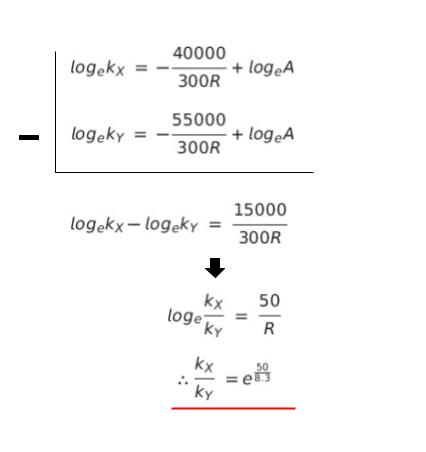
e = 2.7 とあるので、50/8.3 ≒ 6 と評価して 2.76 を計算します。2.73 ≒ 20 なので、2.76 ≒ 400 です。最も近い値を選択肢から探すと 3.9 × 102 です。
以上より、正解は 4 です。
類題 H30no19 活性化エネルギー
https://yaku-tik.com/yakugaku/km-30-19/

コメント