問 題
下図は、ある純物質のエントロピーの温度依存性を示したグラフである。純物質の状態に関する記述のうち、正しいのはどれか。2つ選べ。
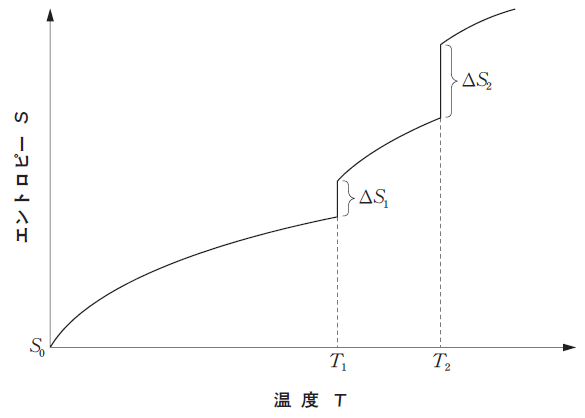
- 物質の温度Tが0 < T < T1の領域では、気体の状態にある。
- 物質の温度TがT1 < T < T2の領域では、固体の状態にある。
- 温度ゼロにおけるエントロピー(S0)は、物質によっては負になる場合がある。
- ΔS2・T2の大部分は、気化エンタルピーの変化量に由来する。
- 物質によらず、ΔS1・T1 < ΔS2・T2の関係が成り立つ。
正解.4, 5
解 説
選択肢 1,2 ですが
エントロピーとは、簡単にいえば乱雑さの指標 です。純物質において熱を与えると、だんだん物質が熱を受け取り、エントロピーは大きくなります。途中で「同じ温度 T で、ある程度の熱を一気に受け取っている」ところは、固体→液体 のような 相変化 を表していると考えられます。このグラフでは、0 ~ T1 が「固体」、T1 ~ T2 が「液体」、T2 ~ 「気体」 を表しています。よって、選択肢 1,2 は誤りです。
選択肢 3 ですが
純物質なので、エントロピーは 0 K で 0 です。熱力学第三法則と呼ばれます。「混合物」だと0Kで、0に近いけど、0にならないことがある。「イオン」だと、見かけ上、負がありえる。ということから「純物質」という限定があるみたいです。
選択肢 4,5 は、正しい選択肢です。
選択肢 5 の記述は、固体から液体になる「融解熱」と、液体から気体になる「蒸発熱」を比べると液体から気体になる方が、熱がいっぱい必要だよね。ということを不等式で表現しているものです。
以上より、正解は 4,5 です。

コメント