問 題
式は、相転移温度と圧力の関係を表したクラペイロンの式である。相転移に関する記述のうち、正しいのはどれか。2つ選べ。
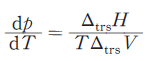
- p:圧力
- T:温度
- ΔtrsH:相転移に伴うエンタルピー変化
- ΔtrsV:相転移に伴う体積変化
- 固体と液体が共存する状態では、純物質は圧力をかけると固体から液体へと変化する。
- 純物質は、圧力が高くなると沸点が上昇する。
- 純物質の状態図における昇華曲線の傾きは負となる。
- 相転移に伴うエンタルピー変化と相転移温度から、相転移に伴うエントロピー変化を求めることができる。
正解.2, 4
解 説
一般的な相図は、横軸に温度 T、縦軸に圧力 P をとると以下のようになります。

固体と液体が共存するのは、固液境界線におけるようなTとPの時です。(一例として、グラフにおける◯の部分)ここで P が増加すると、点で表している状態は上に移動するので、物質は固体になると考えられます。よって、選択肢 1 は誤りです。
選択肢 2 はその通りの記述です。
すなわち、圧力が高いと、より状態は上に移動するので、固体と液体や液体と気体の境界線は、より右側になります。つまり、気体になるための温度がより高くなるので、圧力が高くなると沸点が上昇するといえます。(相図でわかりにくければ、圧力が高い→ぎゅっと押し付けられている→気体になるというのは、粒子がそれぞれ自由に動けるということ→よりエネルギーが必要になる→より温度が高い必要があるぐらいで考えてもよいと思います。)
昇華曲線とは、固体と気体の境界線のことです。一般的に傾きは正です。よって、選択肢 3 は誤りです。
選択肢 4 はその通りの記述です。
エン「トロ」ピー変化 ΔS は、エントロピーの定義から ΔS = q/T です。参考)物理化学まとめ エントロピー
ここで、q は相転移に伴う熱量なので「相転移に伴うエンタルピー変化」です。よって、q と T がわかれば ΔS が求められます。つまり、相転移に伴うエンタルピー変化(q)と、相転移温度(T)から相転移に伴うエントロピー変化を求めることができます。
以上より、正解は 2,4 です。

コメント