問 題
CH3COO-、I-、PO43-、SO42-のナトリウム塩を含む試料水溶液がある。この水溶液に図のような分離操作を行ったとき、沈殿 A 、沈殿 C として分離されるイオンの組合せとして最も妥当なのはどれか。
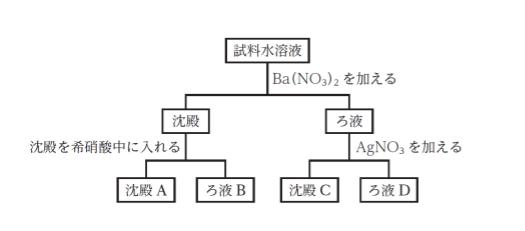
沈殿A 沈殿C
1.CH3COO- PO43-
2.PO43- CH3COO-
3.PO43- I-
4.SO42- CH3COO-
5.SO42- I-
正解 (5)
解 説
Ba2+ イオンといえば、硫酸塩(BaSO4)が白色沈殿で不溶性です。希硝酸(程度)では溶けないだろうと考えられます。従って、沈殿 A で分離されるイオンは SO42- と考えられます。正解は 4 or 5 です。
右側ですが、Ag+で沈殿といえば AgCl↓(白)が基礎知識です。ハロゲン化銀については「AgF 以外水に不溶」が知識です。これを知らなくても AgCl から推測することで、I はハロゲンだし、同様に沈殿と考えられるのではないでしょうか。従って、沈殿 C で分離されるのは、I–です。
以上より、正解は 5 です。

コメント