問 題
Fe2+ の錯体において,[Fe(H2O)6]2+ は磁性をもつが,[Fe(CN)6]4- は磁性をもたない。この違いは中心金属イオン Fe2+ の 3d 軌道の電子配置に起因している。
図 A~D は,Fe2+ の 3d 軌道の電子配置の模式図であり,軌道が配位子によって eg 軌道と t2g 軌道に分裂したときの d 電子の配置及びスピンの方向を示している。ΔE1,ΔE2 は分裂エネルギーの大きさ(ΔE1 >ΔE2)を示し,eg 軌道,t2g 軌道はそれぞれ 2重, 3 重に縮重している。
[Fe(H2O)6]2+ 及び[Fe(CN)6]4-の 3d 軌道の電子配置を表すものの組合せとして最も妥当なのはどれか。
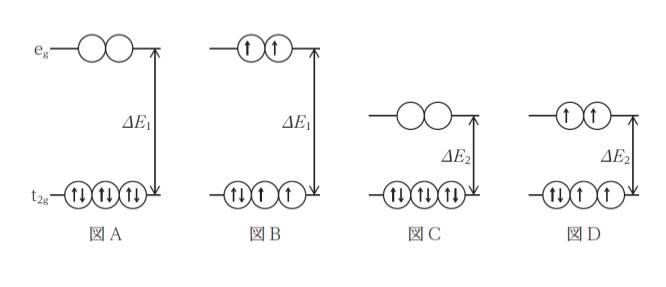
[Fe(H2O)6]2+ [Fe(CN)6]4-
1. 図B 図A
2. 図B 図C
3. 図D 図A
4. 図D 図B
5. 図D 図C
正解 (3)
解 説
配位子が結晶場分裂に及ぼす効果のリストを分光化学系列と呼びます。系列が非常に大きい方からCO>CNー>・・・>ハロゲン です。CN が配位子である方が効果が大きいため、ΔE が大きくなります。従って、[Fe(H2O)6]2+ は図 C or 図D です。[Fe(CN)6]4- は図A or 図 B です。これらの組合せから、正解は 3 or 4 です。
そして、磁性を持つ方は、スピンの方向が揃っているはずであり、逆に磁性が無い方は、スピンの方向が揃っていないはずです。従って、磁性のない[Fe(CN)6]4- は、図 B ではなく図 A と考えられます。
以上より正解は 3 です。

コメント