各種金属イオンの溶解度とpHの関係は下図のように表される。金属イオンを含む排水の処理に関する記述として、正しいものはどれか。
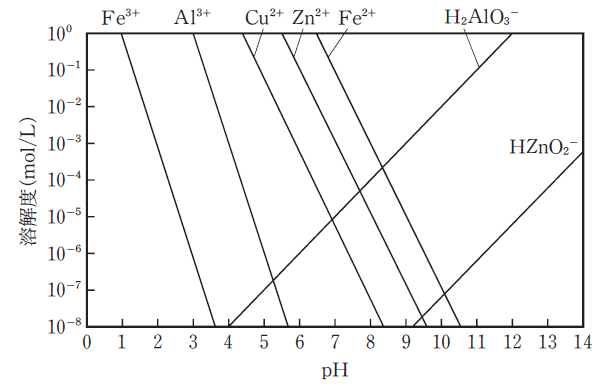
- 銅はpH4付近でほぼ完全に沈殿除去される。
- 鉄は両性金属である。
- アルミニウムはpH9~10でほぼ完全に沈殿除去される。
- 亜鉛はpH13付近でほぼ完全に沈殿除去される。
- 3価の鉄はpH4付近でほぼ完全に沈殿除去される。
正解 (5)
解 説
(1)について、「ほぼ完全に沈殿除去される」というのは溶解度が極端に低いということです(図の下端)。銅(Cu2+)の場合は直線と図の下端とがpH8.3くらいの場所でぶつかっているため、pH8.3あたりで完全に沈殿除去されます。
(2)で、両性金属といえば、アルミニウム、亜鉛、スズ、鉛です。俗にいう「ああ、すんなり」です。ちなみに、これ以外にクロムも両性金属です。クロムが出題されることもあるので、併せて押さえておく必要があります。
(3)のアルミニウムは(2)で解説したように両性金属であり、図中にAl3+とH2AlO3–の2種類の線があります。
つまり、酸性下ではAl3+になっていて、pH6に近づくにつれAl3+は水に溶けなくなっていくのですが、一方でpH4あたりからじわじわとH2AlO3–の形で再溶解していくということです。
pH9~10の範囲を見ると、Al3+の形では存在しないといえますが、一方でH2AlO3–のほうはかなり高い濃度であり、水にしっかり溶け込んでいます。よって、これではほぼ完全に沈殿除去されるとはいえないので、(3)は誤りです。
(4)の亜鉛も(3)のアルミニウムと同様、両性金属です。図を見るとZn2+とHZnO2–の2種類があります。pH13付近ではZn2+の形では存在しないものの、HZnO2–として再溶解していることが読み取れるので、これも誤りです。

コメント