メタンとCOの混合ガスの理論空気量が6.67m3N/m3Nであるとき、混合ガス中のメタン濃度(vol%)はおよそいくらか。
- 40
- 50
- 60
- 70
- 80
正解 (3)
解 説
メタンの燃焼は、以下の化学反応式で示すことができます。
![]()
この問題では混合ガス中のメタンの割合が問われているので、これを仮にaとします。混合ガス全体を1とするため、メタンがaなら、COは(1-a)で表すことができます。また、上式より、ここで消費する酸素は2aです。
一方、COの燃焼は、以下の化学反応式となります。
![]()
上記の通りCOが(1-a)なので、消費する酸素は1/2(1-a)です。
ここで、問題文の「理論空気量が6.67m3N/m3N」という言葉の意味を考えます。これは、混合ガスを完全燃焼させる際にちょうど必要となる空気の量のことです。空気量が6.67m3Nであるとき、そのうち21%が酸素なので、酸素量は6.67×0.21=1.4m3Nとなります。
よって、以下のような式を解けばaが算出できます。
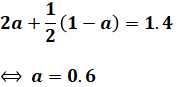
ここで、aは混合ガス中のメタンの割合なので、0.6=60%が答えです。

コメント