前項での説明の通り、芳香族化合物では置換反応が起こりやすいです。置換反応は大きく分けて求電子置換反応と求核置換反応がありますが、この項では求電子置換反応について扱います。
芳香族求電子置換反応の反応機構
芳香族化合物に対して求電子剤を作用させると、芳香環の水素が別の原子(原子団)に置換されます。反応機構は以下の図の通りで、まずは求電子剤が付加して、その後にプロトンが脱離します。
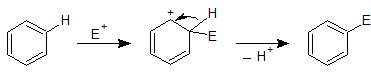
上記の E+ は求電子剤(electrophile)を指しています。付加の後に脱離が起きるこのような反応機構を、付加-脱離機構と呼ぶこともあります。
ハロゲン化
FeCl3 や FeBr3 などのルイス酸存在下でベンゼンにハロゲン(塩素や臭素)を反応させると、置換反応が進行します。
反応機構は先述の通りですが、ここではルイス酸が触媒として反応の進行を助けています。
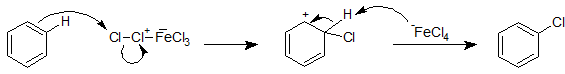
ニトロ化
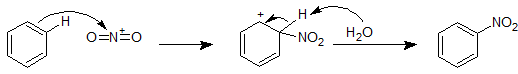
ベンゼンに濃硝酸+濃硫酸を作用させるとニトロベンゼンが生成します。
硝酸はニトロ基(-NO2)の供給源となり、硫酸は硝酸を反応性のあるニトロニウムイオン(NO2+)に変えるための酸性触媒となります。
スルホン化
ベンゼンに濃硫酸を作用させるとベンゼンスルホン酸が生成します。
スルホン化は、上述のハロゲン化やニトロ化と反応機構は同様ですが、可逆反応であることに注意してください。
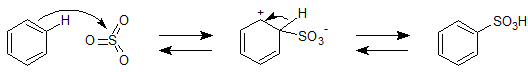
演習問題)99回薬剤師国家試験 問7

コメント