溶解とは、溶媒に気体、液体、固体が溶けて、均一な混合物である溶液になる現象のことです。以降、固体(薬物)の溶解について話をします。
固体の溶解においては、溶解熱の出入りを伴います。固体が溶媒中に溶解する量の上限値のことを溶解度と呼びますが、この溶解度は、温度と溶解熱の関数で表されます。すなわち、以下の式が成立します。

固体の溶解現象は、崩壊、分散を伴いながら溶解します。溶媒に溶け込む溶解速度は、大きい粒よりも顆粒が、顆粒よりも粉末の方が速いです。これは、溶媒と触れる表面積の量が大きいからです。
固体の溶解過程は、層状に、固体→飽和溶液→拡散層→内部溶液としてモデル化されます。このモデルに基づく式がNernst-Noyes-Whitney(ネルンスト・ノイエス・ホイットニー)の式 及び Noyes-Whitney(ノイエス・ホイットニー)の式です。
すなわち、溶解現象が拡散律速であるとして拡散層を仮定し、溶解速度に関する種々のパラメータの関係を表す式です。以下のような式(Nernst-Noyes-Whitneyの式)になります。

上の式において、k = D/Vδ とおいた式が Noyes-Whitney の式です。以下の式になります。
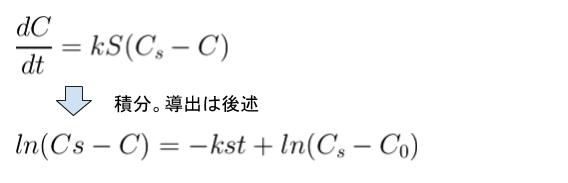
Noyes-Whitneyの式の微分型から積分型への導出は以下のようになります。Cs は溶解度なので、定数扱いであることに注意が必要です。

又、溶解による固体表面積の減少を考慮に入れた式が、Hixson-Crowell(ヒクソン-クロウェル)式です。Hixson-Crowell式では、2つの条件が仮定されています。すなわち、初期濃度が溶解度よりはるかに小さいこと(シンク条件と呼ばれます)と、粒子径一定の粒子が、球状を保ちつつ溶解するという仮定です。以下の式になります。

初期質量と、ある程度時間が経過した時の質量を測定することにより、k を求めることができるという点がポイントです。
補足 Hixon-Crowell 式の導出過程
※ 国試対策としては、全く不要です!
粒子の溶解のイメージは、以下のようになります。
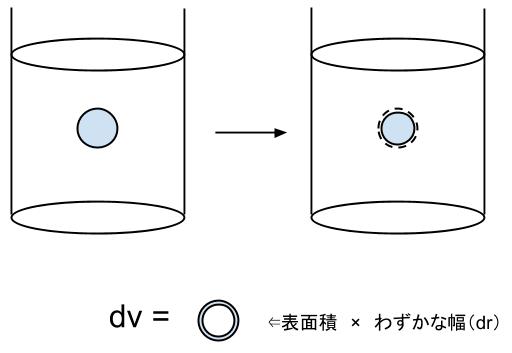
実際には、粒子は1個ではないので、N 個あるとすれば
と表すことができます。
一方で、溶解現象なので、この節で解説した Nernst-Noyes-Whitney の式
も成り立ちます。この式から、少しアプローチします。
Cs>>Cという仮定をおくことにより、Cs-C ≒ Cs とおきます。すると、以下の式になります。
少し、式の形を変形させると
です。
この式の左辺 VdC は、(dV)C とすれば、(微小体積)×(濃度)なので減少した質量といえます。 つまり -dW = VdC です。一行にまとめると
となります。これで、dW と、t が、何か関係があるような式になってきました♪
次に、dW(質量の減少量) = ρdv(密度×減少した体積) 及び、S=N × 4πr2(粒子がN個なので、N × 表面積 です)を代入すると、以下の式になります。
ここで、一番始めに表した式である
を用いて、式を簡単にします。ちょっと見た目を変えて
としておきます。
すると
の形を変えて
とすれば、左辺を -dr とすることができるので
となります。
t = 0 → t = t
r = r0 → r = r の範囲で、上の式を積分すると
文字はいっぱいですが、結局積分する変数が、左辺にも、右辺にも入っていないので、1を x で積分したら x であるように、左辺は r 右辺は t をつけて定積分の計算になります。式は以下のようになります。
計算すると
となります。
後は、この r0 と r を、W0 、W にすれば、終了です!
粒子径と、重さの間には、粒子が N 個なので
がなりたちます。これを、r について解きます。すると
※ r0 = の時は、W0 とします。これを代入すると
です。ほぼゴールです!形をあわせていきます。共通因数をくくりだします。
右辺の分母・分子に、3√(4ΠρN)δρをかけます。右辺は、√では無い方がわかりやすいので、指数で表します。
後は、定数部分の処理です。抜き出すと
です。
分母を3(整数)にするために
何とかして、36を3乗の形にするために
とすることで
となるので、定数項の処理も終わりです。

コメント