状態図とは、物質が温度や圧力の変化に対してどのように相を変えるかを示す図のことです。相図ともよばれます。相図における曲線部分の傾きを式で表したのが、3-1 1)で出てきた Clausius-Clapeyron の式です。
一成分系、及び二成分系の状態図の例をあげます。
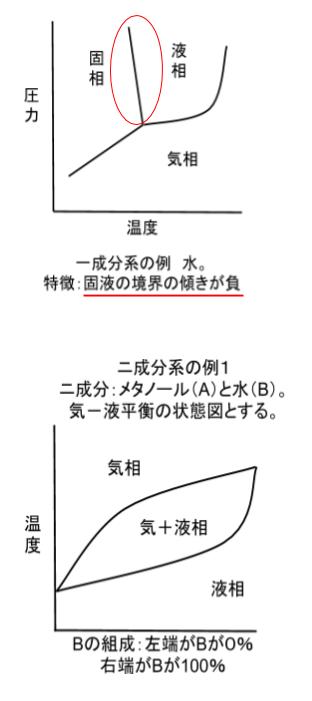
上の図は、水の相図です。水の相図の大きな特徴が、固ー液境界(融解曲線)が負の勾配を示す点です。「温度が上がってるのに、圧力が下がる」と考えると、特徴的であることが実感できるのではないでしょうか。
下の図は、二成分系として、水とメタノールの混合物についての相図です。成分が複数になった場合、どちらが何 % 含まれるか という変数が軸になることが多いです。ニ成分系の状態図では、各点における状態をイメージできるかどうかが重要です。図におけるいくつかの点を例にあげ、詳しく説明します。
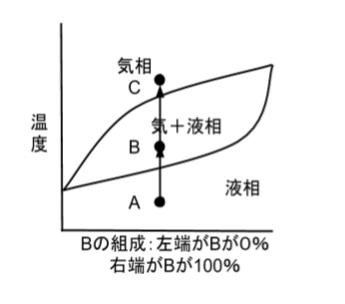
図において、点Aは「メタノールと水の混合溶液が、ある温度において、混合した液相として存在している」状態です。メタノールが何%で、水が何%入っているかは、横軸を読むことでわかります。又、温度は縦軸を読むことでわかります。
次に、液体をだんだん加熱していったとします。メタノールと水の混合割合は変わらず、温度だけが上がっていくため、混合液体の加熱は、状態図において上に点が移動していく形で表現されます(図でいう点A→点B)。ある温度以上になると、液相+気相となります。すなわち、沸点の低い方(この例ではメタノール)が主に蒸発し始めます。注意すべきは、この蒸気にはわずかですが、水蒸気も含まれるということです。
ここで点 B について詳しく見ていきます。点 B の状態は「メタノールと水の混合溶液が、ある温度において、液相と気相として存在している」という状態です。この時、液相も気相も、先程の点 A の時とは組成が変化しています。(液相は、蒸発しやすいメタノールがどんどん蒸発するため、水の割合が多くなる。気相の組成は、メタノールの方が蒸発しやすいため、メタノールの割合が多くなる。)
相図では、この液相及び気相の組成について読み取ることができます。点 B からまっすぐ左右に線を引き、曲線と交わる点が、液相+気相における液相及び気相の組成を表しています。以下、次の図を使って説明します。
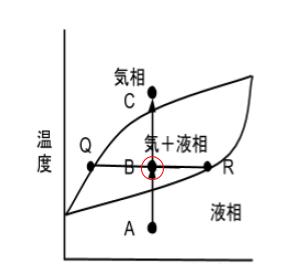
図において、点 Q が気相を、点 R が液相を表します。どっちが気相でどっちが液相かというのは覚えてもよいのですが次のように考えるのがおすすめです。「点 Q は、Bの組成が低い」→「A の組成が多い」→「メタノールが多い」→「先に蒸発するのはメタノール」と考えて、Qが気相です。
又、この気相と水相の「存在量の比」というのが、線分 QR の、点 B から見た”足の長さ”により表されています。具体的には、気相 Q と液相 R の存在量の比は、RB(こっちが気相):BQ(こっちが液相)です。
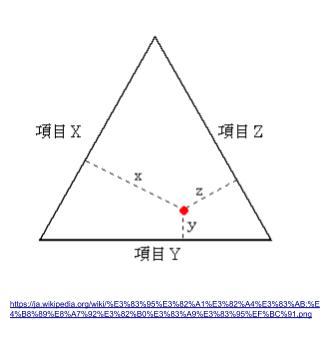
三成分系においては、三角図を読みとることが必要になります。三角図とは下のような図で、三成分の比を表すことができる図です。

コメント