問 題
正逆反応とも一次反応で進行する反応を考える。
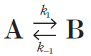
k1=0.01min-1、k-1=0.02min-1のとき、反応物Aと生成物Bの割合は時間とともにどのように変化するか。1つ選べ。ただし、反応開始時の反応物Aの割合を1とする。
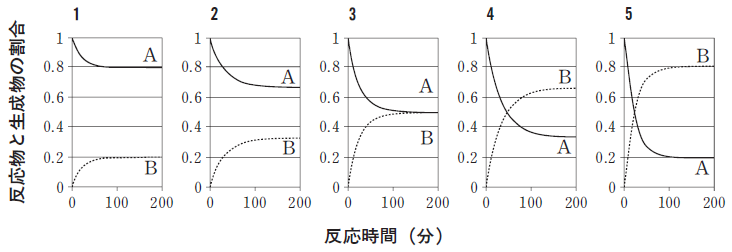
正解.2
解 説
一次反応で進行する ということから、A → B の反応速度は v = k1 [A] つまり、v = 0.01 [A] と表すことができます。同様に、B → Aの反応速度は v’ = k-1 [B] つまり、v’ = 0.02 [B] と表すことができます。v = v’ つまり 0.01 [A] = 0.02 [B] となる時、見かけ上反応が止まります。0.01[A] = 0.02[B] は、両辺を 100倍すれば [A] = 2[B] です。
つまり、反応が止まった時に [A] : [B] が2:1 になっているグラフを選べばよいということになります。以下、各選択肢を検討します。
選択肢 1 ですが
[A]:[B] が4:1なので、誤りです。
選択肢 2 は、正しい選択肢です。
選択肢 3 ですが
[A]:[B] が 1:1なので、誤りです。
選択肢 4,5 ですが
反応が止まった時に、B の方が濃度が高くなっており、明らかに誤りです。
以上より、正解は 2 です。

コメント