問 題
次の可逆反応について考える。
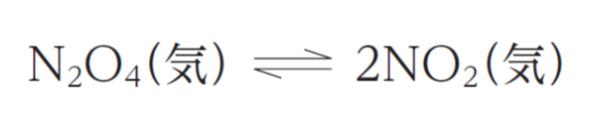
N2O4 (気) 及び NO2 (気) の標準生成エンタルピーはそれぞれ 9.2 kJ・mol-1、33.2 kJ・mol-1 である。この可逆反応が標準状態で平衡状態にあるとき、㋐、㋑、㋒ の操作をそれぞれ行った。このとき、平衡が右側に移動する操作として妥当なもののみを全て挙げているのはどれか。ただし、N2O4 (気) 、NO2 (気) 及び Ar (気) は理想気体であるものとする。
㋐ 反応系の温度と体積一定で Ar (気) を加える。
㋑ 反応系の圧力一定で加熱する。
㋒ 反応系の温度と圧力一定で N2O4 (気)を加える。
1.㋐
2.㋐、㋑
3.㋑
4.㋑、㋒
5.㋒
正解.4
解 説
㋐ ですが
温度、体積一定で Ar が加わると、圧力増加です。そのため、圧力が減少する方向に平衡が移動します。圧力が減少する方向とは、反応式の係数の和が減る方向なので、左に平衡が移動します。㋐ は右側に移動する操作ではありません。
㋑ は妥当です。
加熱なので、吸熱反応の方向に平衡が移動します。N2O4 → 2NO2 が吸熱反応であることは、基礎知識と考えられます。
㋒ は妥当です。
N2O4 が増えたので、N2O4 を減らす方向である 右方向に平衡が移動します。
以上より、正解は 4 です。
類題 R1no18 平衡定数
https://yaku-tik.com/yakugaku/km-r1-18/

コメント