電気滴定とは、電位差や電極間を流れる電流値の測定により滴定終点を読み取るような滴定のことです。
電位差滴定法は、電位差を測定することにより滴定終点を読み取る方法です。今までの項目で説明してきた滴定の種類により、指示電極と呼ばれる使用する電極の種類が異なります。
中和滴定や非水滴定では、ガラス電極を使います。沈殿滴定では、銀電極を使います。酸化還元滴定では、白金電極を使います。キレート滴定では、水銀-塩化水銀電極を使います。
電流滴定法は、電流の変化を測定することにより滴定終点を読み取る方法です。指示電極には、白金が用いられます。酸化還元滴定の一種であるジアゾ化滴定が、代表的な電流滴定法を用いる滴定です。
電量滴定法は、滴定試薬を電気分解により発生させて滴定反応を行うという方法です。終点に達すると、滴定試薬の発生が止まります。要した電気量から、目的成分を定量します。代表的な電量滴定法は、カール・フィッシャー法という水分の定量法です。
ヨウ化物イオンを混合した、水分測定用の試液を用い、電解により反応に必要なヨウ素を発生させます。終点に達すると、過剰のヨウ素が電極により検出され電流が止まります。反応式は、下のようになります。
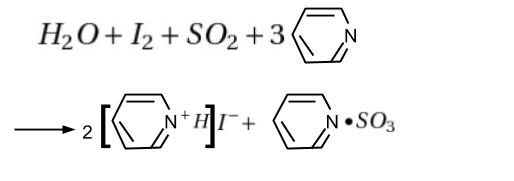
※ 生成物のうち、右側の分(ピリジン・SO3)は、さらに試液に含まれるメタノールと反応して塩を形成します。
最後に、導電率滴定法について説明します。水溶液中での電流の流れやすさを測定することで滴定の終点を見分ける方法です。導電率は、κ(カッパ)で、よく表されます。ここで、抵抗率を ρ(ロー)、抵抗をR (単位は Ω)、電極の断面積をA (単位は m2)、電極間の溶液の長さを l (単位は m) とおくと
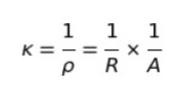
が成り立ちます。

コメント