マススペクトルでは測定対象の分子をイオン化することが欠かせませんが、その際に分子の構造を壊さずにそのままイオン化できることもありますが、大抵は化合物のどこかの結合が切れてしまいます。
そのように結合が切れることをフラグメンテーションといい、それによってできた化合物の破片のことをフラグメントイオンといいます。
このフラグメントイオンの質量の情報から、測定対象である分子がどのような部分を持つか(たとえば、メチル基を持っている、ベンゼン環を持っているなど)が多少わかってくるので、フラグメンテーションで得られた情報も構造決定のヒントとなることが多くあります。
この項では、4種類のフラグメンテーションについて紹介していきます。
ラジカル開裂
フラグメンテーションの中でも最も代表的なものがラジカル開裂です。これは、単結合を形成する2つの電子が開裂する際、1つずつの電子に分かれてラジカルを生成するような開裂です。
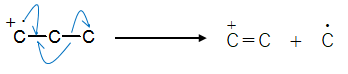
開裂しやすい結合というのは決まっていて、具体的には R-CH2OH や R-CH2NH2 の「R-C」間の結合が挙げられます。
つまりはヘテロ原子のα位の炭素とβ位の炭素の間の結合がラジカル開裂を起こしやすいということですが、これは、開裂後のラジカルが比較的安定しているためです(「C-O」間や「C-N間」ではなく、「C-C間」です)。
ほかには、ベンジル位 Ph-CH2-R の「C-R」間やアリル位 CH2=CH-CH2-R の「C-R」間も、同様の理由でラジカル開裂をしやすくなっています。
特にベンジル位で開裂した場合、Ph-CH2 のため m/z = 91 となるので、わかりやすく構造決定のヒントになります。
また、アルキル基がフラグメンテーションを起こすときには、やはりラジカルの安定性から、第4級炭素や第3級炭素でラジカル開裂を起こしやすく、第1級炭素ではあまり開裂が起こりません。
ちなみに、二重結合や芳香環では結合を2本切らないとフラグメントイオンにならないこともあり、エネルギー的に不利なので、これらがフラグメンテーションを起こすことは基本的にありません。
イオン開裂
イオン開裂はラジカル開裂とは対照的で、単結合を形成する2つの電子が開裂する際、2つともが一方の原子に移動して、アニオンまたはカチオンを生成するような開裂の仕方です。
McLafferty転位
McLafferty転位(マクラファティー転位)というのは、以下のような六員環遷移状態を経て起こるα-β位間での開裂です。
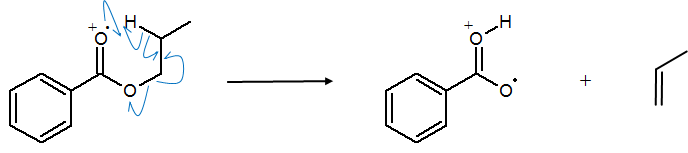
四員環転位
McLafferty転位は六員環遷移状態を経て起こるα-β位間での開裂でしたが、四員環転位は四員環遷移状態を経て以下の図のように水素転位が起こる開裂です。
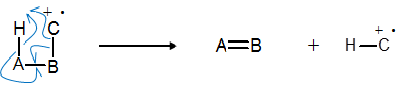

コメント