問 題
塩基性が最も強い含窒素化合物はどれか。1つ選べ。
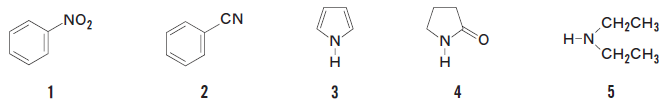
正解.5
解 説
塩基性を持つためには、その構造に孤立電子対を持っている必要があります。(参考 有機化学まとめ ルイス酸・ルイス塩基)。
N 原子は価電子が 5 であり、3 つの原子と結合しても孤立電子対を有するため、アンモニアやアミンは塩基性を示します。
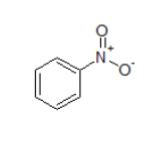
選択肢 1 はニトロベンゼンであり、以下の図のとおり N 原子は孤立電子対を有していません。
よって、これは塩基性ではありません。
選択肢 2 はベンゾニトリルです。
シアノ基(ニトリル基)は N 原子が sp 混成軌道であり、sp2 や sp3 に比して電子が原子核に引き寄せられているので塩基性は弱くなります。
選択肢 3 はピロールです。
N原子は非共有電子対を有していますが、これが芳香性を保つために使われている(=環全体に非局在化されている)ために塩基性ではありません。
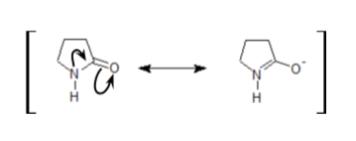
選択肢 4 はアミドです。
アミドは以下に示すように非共有電子対が非局在化しているため、これも塩基性はかなり弱いです。
選択肢 5 がこの 5 肢の中で唯一、普通のアミン(第二級アミン)です。これは非共有電子対を有し、はっきりと塩基性なので正解となります。
以上より、正解は 5 です。

コメント