問 題
実在気体の分子半径に関する、次の記述の㋐、㋑、㋒に当てはまるものの組合せとして最も妥当なのはどれか。ただし、アボガドロ定数を6.0×1023mol-1とする。「圧力 P、モル体積 Vm、温度 T の実在気体の状態方程式として
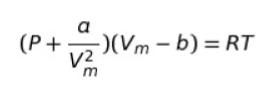
で表されるファンデルワールスの式がある。ここで R は気体定数であり a、bはファンデルワールス定数である。a、bのうち ( ㋐ ) は気体分子 1mol 当たりの排除体積を表している。
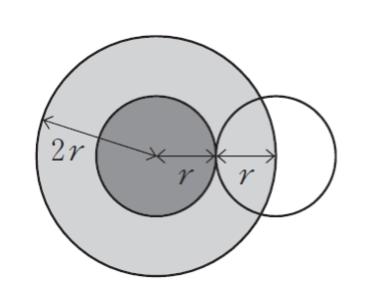
排除体積を分子レベルで考える。気体分子を半径 r の球として考えると、図のように、気体 2 分子において一方の分子の網掛け部分すなわち半径 2r の球の部分より近くには他の分子の中心は侵入できない。つまり他分子を排除している。よって、1 分子当たりにすると、気体分子の体積の( ㋑ )倍が排除体積となる。
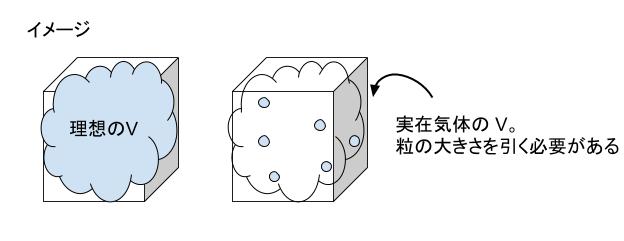
ヘリウムの a、b はそれぞれ 3.45×10-3 Pa・m6・mol-2 及び 2.37×10-5 m3・mol-1 である。ヘリウムの原子半径を r0〔m〕とすると、r03 = ( ㋒ )m3 となる。」
㋐ ㋑ ㋒
1.a 4 3.5×10-28
2.a 8 2.4×10-30
3.b 4 2.4×10-30
4.b 4 1.4×10-29
5.b 8 3.5×10-28
解 説
【㋐について】
実在気体の体積を調整する項は「ーb」です。これは知識です。正解は 1~3 です
【㋑について】
・気体分子の体積 = 半径 r の球の体積 ∴V = 4/3 πr3
・排除体積 = 半径 2r の球の体積 = 4/3 π(2r)3 = 8V(∵V = 4/3 πr3)。気体 2 分子において、排除体積が 8V なので、1 分子あたりでは 4V となります。正解は 3 or 4 です。
【㋒について】
㋐より、b が 1 mol あたりの排除体積と書いてあるので、2.37 × 10-5 が 「1 mol あたり排除体積」です。
㋑で計算したのが、「1分子あたりの排除体積」なので、1分子あたりなら排除体積は 4V = 4×4/3 πr3 と表すことができています。
1mol = 6.0 × 1023 個 なので『2.37×10-5 = 4×4/3 πr03 × (6.0 × 1023 )』が成り立つはずです。この式を、r03 = ・・・の形にすればよいとわかります。選択肢より、それほど厳密な解は不要なので、2.37 ≒ 2.4、 π ≒ 3 と近似して見ると
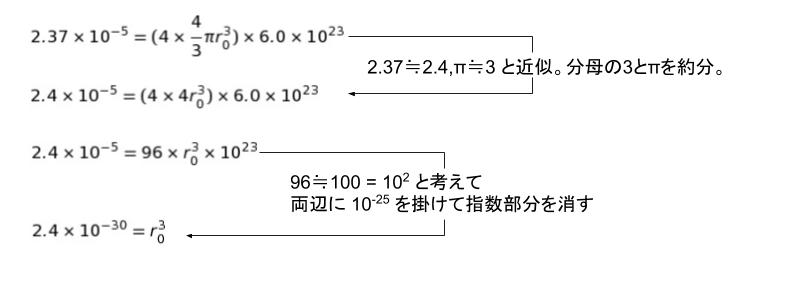 となります。
となります。
以上より、正解は 3 です。

コメント