問 題
硫化水素 H2S 、二酸化硫黄 SO2 、三酸化硫黄 SO3 の気体分子の形を組み合わせたものとして、最も妥当なのはどれか。
H2S SO2 SO3
1, 折れ線 折れ線 平面三角形
2, 折れ線 直線 平面三角形
3, 折れ線 直線 三角錐
4, 直線 折れ線 三角錐
5, 直線 直線 三角錐
正解 (1)
解 説
まず H2S ですが、これは S≒O とすれば、H2O と同じ形、つまり折れ線形だろうと判断できます。正解は 1 ~ 3 です。
次に、SO2 のルイス構造式を考えてみれば、S の最外殻電子が 6 なので、CO2 と比較した時に孤立電子対が1つ余るとわかります。
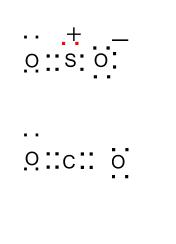
電子対同士は、できるだけ離れようとするので、直線ではないだろうと判断できます。※ CO2 の形が直線形であることは基礎知識です。
以上より、正解は 1 です。

コメント