問 題
一定質量の理想気体を、圧力 p1、温度 T1 の状態 ① から、体積一定のまま、圧力 p2、温度 T2 の状態 ② になるまでゆっくりと変化させたとき、p2 として最も妥当なのはどれか。ただし、T2 > T1 とする。
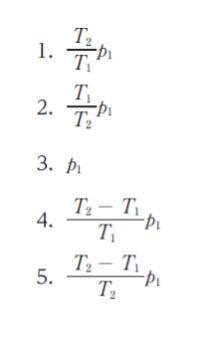
解 説
理想気体が出てきたら状態方程式 PV = nRT です。物質量 n について、選択肢を見ても触れられていないため、n = 1 とします。また、体積一定のままとあるので、V は変化しません。
状態 ① において、状態方程式より p1V = RT1 ・・・(1)が成り立ちます。また、状態 ② において同様に、状態方程式より p2V = RT2 ・・・(2)です。
問題文と選択肢から、本問は要するに「p2 を p1,T1,T2 で表してみてね」という問題です。式変形の1例としては、まず p2 = … とした上で、余計な R/V 消去という流れになります。答えがあえば、式変形の流れは自分なりでかまいません。

p2 = p1 T1/T2 となるので、正解は 1 です。
【別解】
「理想気体ときたら状態方程式」を忘れていた場合でも、諦めず具体的に考えるとよいです。
限りなく T2 と T1 が近い温度としてみます。T1 = 30℃ で T2 = 30.00000001 ℃ のような設定です。もうほぼ同じなので、T1 ≒ T2 と近似します。
条件をほとんど変えていないので p1 ≒ p2 となるはずです。選択肢を見ると、選択肢 4,5 は T1 ≒ T2 の時 ほぼ0になってしまいます。従って、選択肢 4,5 は誤りです。
次に、とてつもなく T2 を大きくした場合を考えます。「体積一定ですごく温度を上げる」→「圧力はとても大きくなるはずだ」という想像がつくのではないでしょうか。
選択肢 2 では、圧力が下がってしまいます。また、選択肢 3 は T2 に無関係となります。どちらも不適切と考えられるため、選択肢 2,3 は誤りです。
以上より、正解は 1 です。

コメント