問 題
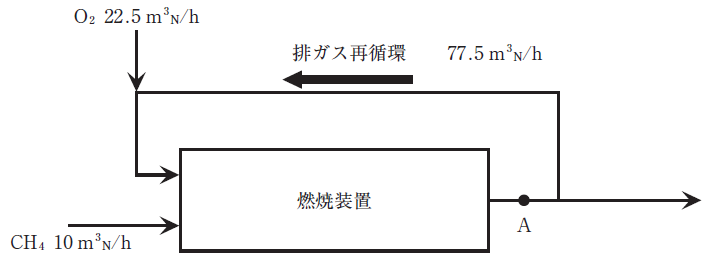
排ガスの一部を水蒸気の凝縮なしに再循環しているラインに酸素を吹き込んで、メタンを完全燃焼させる下図に示すような燃焼装置がある。
図中の運転条件で定常状態が達成されているとき、燃焼装置出口(図中A点)での乾き燃焼排ガス中のCO2濃度は何%となるか。
- 50
- 60
- 70
- 80
- 90
正解 (4)
解 説
問題文に「メタンを完全燃焼」とあるので、まずはこの化学反応式を以下に示します。
![]()
問題の図には燃焼装置と排ガス再循環の経路が載っていますが、これらを下図の青色枠線のように一つの系としてまとめて考えると、この系に入るのはCH4とO2の2種類だけとなります。
また、系の中ではCH4が完全燃焼により消失するので、系から出ていく物質は上記の化学反応で生成するCO2とH2O、それと余ったO2の3種類です。
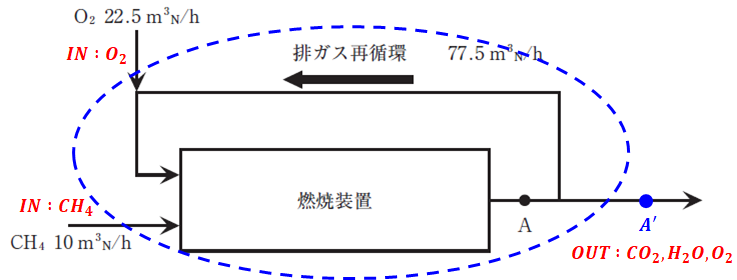
ここで、求めたいのは図中A点での乾き燃焼排ガス中のCO2濃度ですが、A点(燃焼装置出口)でも上図のA’点でもガスの成分や濃度に違いはないので、A’点でのCO2濃度を計算できればそれがそのまま答えとなります。
よって、この問題は、10[m3N/h]のCH4と22.5[m3N/h]のO2を反応させたとき、完全燃焼後の乾き燃焼排ガス中のCO2濃度は何%となるか…という設問と見なすことができます。
上図青枠線に入る物質と出ていく物質の物質収支は次のように表すことができます。
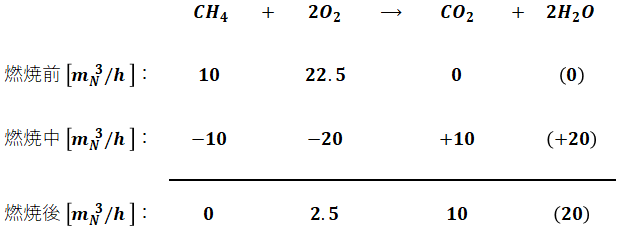
以上より、反応後には2.5[m3N/h]のO2と10[m3N/h]のCO2が残るので、乾き燃焼排ガス中のCO2濃度は次のように計算できます。なお、今回は乾き燃焼排ガスの話をしているので、生成するH2Oは計算に含めない点に注意してください。

よって、正解は(4)です。

コメント