炭素86%、水素14%の組成の灯油の(CO2)max(%)はおよそいくらか。
- 12
- 13
- 14
- 15
- 16
正解 (4)
解 説
最初に気をつけておきたいことは、(CO2)maxというのは「乾き燃焼ガス中のCO2濃度」です。「乾き」なので、水蒸気の分を勘定してはいけません。
それでは、本題に入ります。まず、わかりやすいようにもともとの灯油が1kgあると仮定します(仮定なので、違う数字で考えても差し支えありません)。灯油が1kgなら、問題文より、炭素は860g、水素が140gあることになります。このとき、それぞれの物質量は以下のようになります。
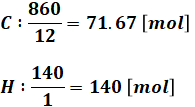
続いて、C、Hをそれぞれ燃焼させる反応式と、消費するO2、生成するガスの物質量を示します。
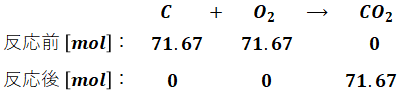
Cが71.67molなので、消費するO2も生成するCO2も71.67molとなります。
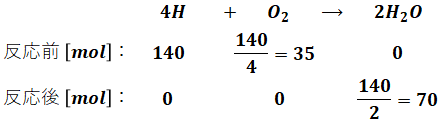
4Hが140molなので、消費するO2は35molです(生成するH2Oは70molですが、これは乾き燃焼ガスでは考えなくて良いです)。
以上から、完全燃焼で消費する酸素量は次のように計算できます。
![]()
酸素は燃焼後にはなくなっているので、問われている(CO2)maxには影響がありませんが、空気中の窒素は反応の前後で増えも減りもしないため、反応後にも元々あった分が残っています。空気の成分は酸素が21%、窒素が79%(アルゴン等の微量物質は気にしません)なので、窒素量は、
![]()
と計算できます。
(CO2)maxは、反応後の全ての気体(ただし乾きなので水分は除く)のうち、CO2の割合を求めればよいので、
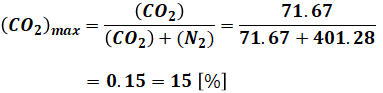
と求めることができます。

コメント