1m3Nのメタンを10m3Nの空気で燃焼させたところ、湿り燃焼排ガス中にCOが1.04%含まれる不完全燃焼を生じた。このとき湿り燃焼排ガス中のCO2濃度はおよそ何%か。ただし、この不完全燃焼では、メタンはすべて反応し、生成物はCO2、CO及びH2Oだけと仮定する。
- 7.1
- 7.4
- 7.7
- 8.0
- 8.3
正解 (4)
解 説
メタンを燃焼させてCOとCO2が生成する式は次のように表すことができます。ただし、下記の化学反応式は係数を入れていない未完成のものです。
![]()
ここで、問題文よりメタンは1m3Nなので、係数を1として考えます。次にCOの係数は不明なのでaと仮定すると、CO2の係数は左辺と右辺のCのバランスを考えると(1-a)となります。H2Oについては、左辺にHが4つあるので、係数を2にすることで右辺のHも計4つになります。この段階で、O2以外の係数が記入できます。
![]()
最後にO2の係数を考えます。右辺には3つの項で酸素が使われていますが、それらの合計と左辺のOの数が一致しなければいけないので、以下のようになります。これで化学反応式は完成です。
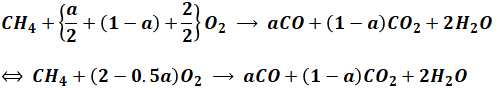
一方、問題文より空気は初めに10m3Nほどあったので、上式のように(2-0.5a)m3Nを使ったとしても、次式の分だけ余りが出ます。これは反応に関与しない空気量(窒素+余った酸素)です。
![]()
メタンは反応によって全てなくなっているため、以上の計算から、反応後に存在する物質の量は次のようにまとめることができます。
- 反応に関与しない分の空気:(8+0.5a)
- CO:a
- CO2:(1-a)
- H2O:2
このうちCOの割合が1.04%ということなので、次のように計算することでaを求めることができます。

最終的に問われているのはCO2の割合なので、今度は分子をCO2にして、aの値を代入すれば、求めたい答えを出すことができます。
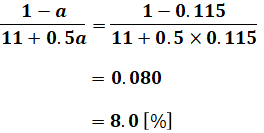
以上から、答えは(4)になります。

コメント