問 題
紫外可視分光法により河川水の鉄(Ⅱ)イオン(Fe2+)濃度を求めたい。Fe2+ を含む水溶液は、フェナントロリン(C12H8N2)を加えると、キレートを生成し赤色を呈する。
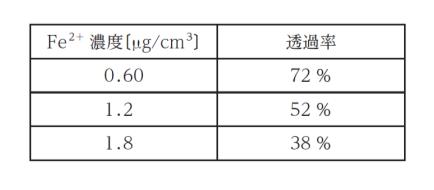
紫外可視分光光度計を用いて、ある波長における透過率を Fe2+ の濃度を変えて測定したところ表のデータを得た。ある河川の水を採取し、同様の操作をして透過率を測定したところ、67 % であった。
この河川水に含まれる Fe2+ の濃度〔μg/cm3〕を求めよ。ただし、ブランク溶液の透過率は 100 % とし、log10 0.38 = ー0.42、log10 0.52 = ー0.28、log10 0.67 = ー0.17、log10 0.72 = ー0.14 とする。
解 説
吸光度を A 、透過率を T とすれば A = -log10T です。これは基礎知識です。これをふまえると Fe2+ 濃度が 0.60,1.2,1.8 の時それぞれ吸光度は 0.14,0.28,0.42 となります。きれいな比例関係にあります。河川水を採取し、透過率が 67% なので、吸光度は 0.17 です。さて、Fe2+ 濃度は なんでしょう?という問題になります。
Fe2+ 濃度が 0.60 増えると 吸光度が 0.14 上がっています。求める濃度を x(μg/cm3) とおけば、x の時 0.17 なので 0.60:0.14 = x:0.17 です。従って 0.14x = 0.102 です。∴x = 0.728… となります。有効数値2桁で丸めれば 0.73 です。

コメント