問 題
炭酸水素ナトリウム水溶液の pH に関する次の記述の ㋐、㋑ に当てはまるものの組合せとして最も妥当なのはどれか。ただし、炭酸の第一解離定数 K1 、第二解離定数 K2 及び水のイオン積 KW について、pK1 = 6.35、pK2 = 10.33、pKW = 14.00とする。
「炭酸水素ナトリウム 1.0×10-2 molを純水に溶かし、全体を 100 mLとした。このとき、炭酸水素イオンは一部が炭酸及び炭酸イオンに変化する。その濃度は、炭酸については
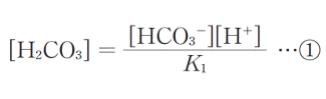
炭酸イオンについては
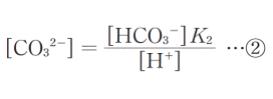
である。炭酸、炭酸水素イオン、及び炭酸イオン全体としては
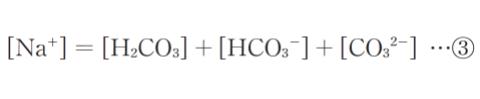
となっており、また、電荷の釣合いより
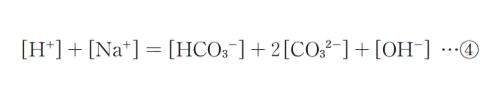
となる。式③、④をまとめ、相対的に十分小さいと考えられるものを無視すると、( ㋐ )となる。この式と①及び②から、pH = ( ㋑ )となる。」
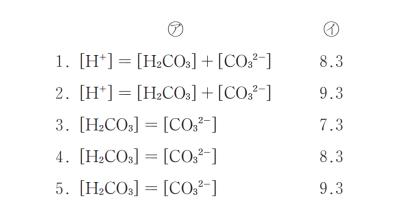
正解 (4)
解 説
問題文の指示に従い、まず③,④をまとめてみます。
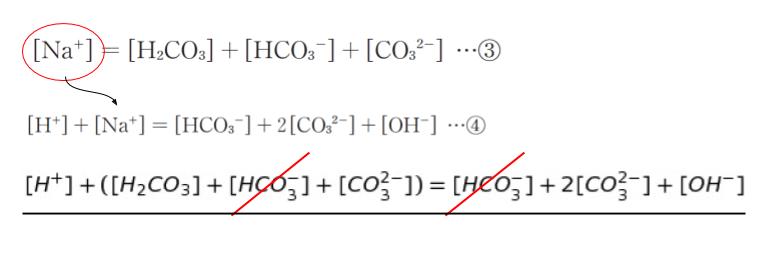
この式から選択肢 1,2 の答えである [H+] = [H2CO3] + [CO3]2- は作れません。その 3 つを残すと符号があいません。よって、正解は 3~5 です。
[H+] 及び [OH–] を相対的に小さいとみなします。①、②、㋐より pH がわかるということなので式を並べてみます。
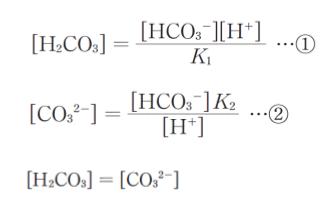
こうしてみると、①の右辺 = ②の右辺 とわかります。[H+]もあるし、うまくpH が出せそうです。

pH = -log10[H+] なので、pH = 8.34 です。
以上より、最も近い選択肢を選べば、正解は 4 です。

コメント