結晶場理論に関する次の記述の ㋐,㋑ に当てはまるものの組合せとして最も妥当なのはどれか。
「孤立した遷移金属イオンの d 軌道は、五重に縮退している。しかし、配位子が遷移金属イオンの周りに配位して化合物を形成するとこの縮退が一部解ける。
例えば、遷移金属イオンを中心とする直交軸上に 6 個の配位子が存在する八面体型の錯体において、五つの d 軌道は eg 軌道と t2g 軌道の二つのエネルギー準位に分裂する。ここで dxy 軌道は ㋐ 軌道に分類される。
Fe3+の 3d 電子は 5 個あり、その配置は八面体結晶場が弱いときと強いときで異なる。弱い八面体結晶場における Fe3+ の 3d 電子の配置は、図 ㋑ のようになる。ただし、図中の ΔO は配位子場分裂パラメーターである。」
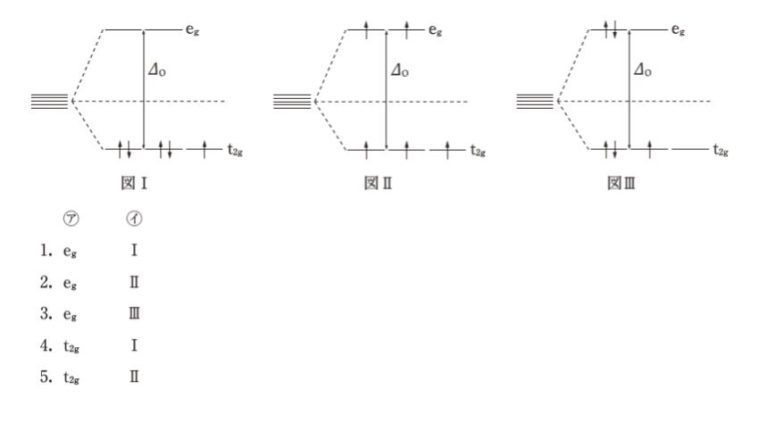
5つの d 軌道は、2 つの eg 軌道 と 3つの t2g 軌道 に分裂します。
eg 軌道とは dx^2-y^2, dz^2 です。
t2g 軌道とは dxy, dyz, dxz です。
これは基礎知識なので、知っているかどうかです。正解は 4 or 5 です。
そして「結晶場」が「強い」 ほど、つまり金属イオン単独よりも配位子がある時の影響が大きい時 ほど「エネルギー準位差が大きく」なります。いいかえると「すっごい居心地のいい軌道と、そうでない軌道にわかれる」 という話です。その場合は、電子がみんな、居心地のいい軌道の方にいきます。
ところが本問では結晶場は弱い とあるので、2つの軌道のエネルギー差がそれほど大きくありません。そのため、まずは安定な方にポンポンと入っていって、その際は Hunt (フント)の規則に則って同じ向きで3つ入っていきます。そして、4つめの電子が「ややぎゅうぎゅうの少しだけ居心地良さげな軌道」ではなく「少し居心地悪いけどガラガラに空いている軌道」へと行き、5つめの電子も同様の決断を、フントの規則に則り同じ向きで入っていきます。従って、弱い八面体結晶場では、3d 電子の配置は 図Ⅱのようになります。
以上より、正解は 5 です。

コメント