問 題
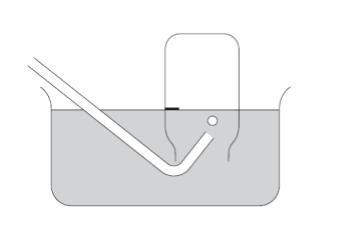
図のように,目盛りを 1 か所付けた集気瓶を用いて,集気瓶内の水面の高さが,集気瓶の目盛り及び水槽内の水面と一致するまで,酸素を水上置換で捕集した。大気圧が P のとき,絶対温度 T1,T2 の条件下でこの捕集を行ったところ,捕集された酸素の質量は,それぞれ,w1,w2 であった。
T1 における水の蒸気圧が P1 のとき,T2 における水の蒸気圧として最も妥当なのはどれか。ただし,室温と酸素及び水の温度は等しく,また,酸素は理想気体として振る舞うものとし,水に対する酸素の溶解度は無視できるものとする。
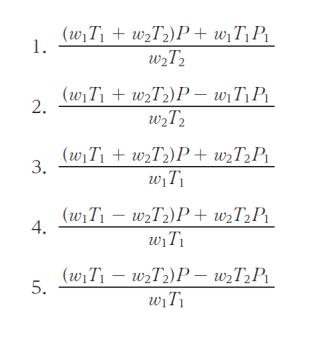
解 説
大気圧 P と、集気瓶内の気体の圧力が等しいと考えられます。集気瓶内の気体の圧力とは、水の蒸気圧+酸素の圧力と考えられます。温度が T1 なら P = P1 + 酸素の圧力です。温度が T2 なら P = P2 + 酸素の圧力です。ここで T1 = T2 の場合を考えます。当然 P1 = P2 です。また、T1 = T2 とした時に w1= w2 です。選択肢を計算すると、それぞれ
1:2P + P1
2:2P ー P1
3:2P + P1
4:P1
5:ーP1 です。P2 = P1 となるのは選択肢 4 のみです。
以上より、正解は 4 です。
ちなみに、一般的に解くと以下のようになります。
酸素の圧力を PO2 とします。PV = nRT が成立します。よって PO2 = nRT/V です。ここで、酸素の分子量を M とすれば、n = w/M です。PO2 = wRT/MV と表すことができます。n,R,V,M については定数です。
温度が T1,T2 の時、それぞれ
P ー P1 = w1RT1/MV ・・・(1)P ー P2 = w2RT2/MV・・・(2) と表すことができます。余計な文字を消して P2 = ・・・の形にします。
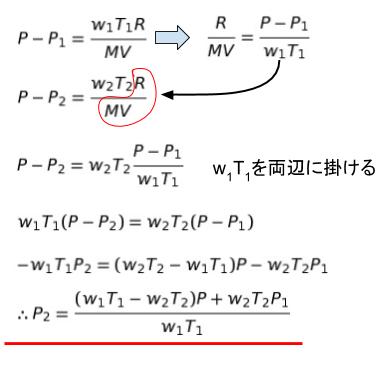
以上より、正解は 4 です。

コメント