問 題
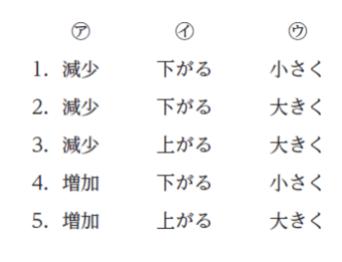
気体の状態変化に関する次の記述の ㋐、㋑、㋒ に当てはまるものの組合せとして最も妥当なのはどれか。
「圧力、温度、体積がそれぞれ互いに等しい同じ種類の理想気体を、一方を可逆的に等温変化、もう一方を可逆的に断熱変化させて、気体の体積を同じだけ増加させた。
このとき、等温変化では気体の温度は変わらないが、断熱変化では、外部にする仕事の分だけ内部エネルギーが ㋐ し、気体の温度が ㋑。よって、変化後の気体の圧力は、断熱変化の方が等温変化より ㋒ なる。」
解 説
【熱力学第一法則】
熱力学第 1 法則 は、ΔU = ΔQ + Δw です。内部エネルギー、仕事ときたらぜひ思い出したい基礎知識です。内部エネルギーの変化量は、気体に加えられた熱量 Q と外部から気体に加えられた仕事 W の和となります。
【理想気体の内部エネルギー】
理想気体の内部エネルギーは、温度依存です。つまり、温度が変化しなければ変化せず、温度が上がれば増加、下がれば減少です。
㋐ ですが
断熱変化では、ΔQ = 0 です。このため、ΔU = Δw となります。つまり「外部にする仕事」の分だけ、内部エネルギーが「減少」します。※外部から気体に仕事が加えられれば内部エネルギーが増加するので、気体が外部に仕事をすれば内部エネルギーは減少する、ということです。
㋐ は「減少」です。正解は 1 ~ 3 です。
㋑ ですが
内部エネルギーが減少すれば、気体の温度は「下がる」です。㋑ は「下がる」です。正解は 1 or 2 です。
㋒ ですが
理想気体 の状態方程式 pv = nRT を考えます。断熱変化でも等温変化でも、体積変化は同じなので左辺の v は同じです。右辺の n,R は定数とみなしてよいです。断熱変化の方が T が減少したので 断熱変化の方が p は小さいとわかります。
具体的に例えば
v = n = 1、T = 300,減少した T = 200 として考えるとわかりやすいです。
断熱変化:p = R × 200
等温変化:p’ = R × 300 と表せるので、断熱変化の方の圧力の方が「小さい」
以上より、正解は 1 です。

コメント