次の(ア)~(エ)の酸化還元系について、標準酸化還元電位の高い順に並んでいるのはどれか。
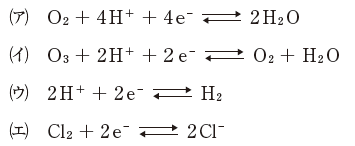
- (イ) > (ア) > (ウ) > (エ)
- (ア) > (イ) > (ウ) > (エ)
- (ア) > (イ) > (エ) > (ウ)
- (イ) > (エ) > (ア) > (ウ)
- (イ) > (ア) > (エ) > (ウ)
正解 (4)
解 説
酸化還元対を含む溶液に白金電極と水素電極とを入れると、両極間に電位差を生じ、これを標準酸化還元電位といいます。標準酸化還元電位の高い系は、より低い系を酸化することができるので、これは酸化剤としての序列をつける問題です。
強い酸化剤として有名なのは、まずオゾン(O3)です。問題文の(イ)に当たります。
次に強いのは過酸化水素水(H2O2)や過マンガン酸塩(MnO4–)です。
まぁまぁ強い酸化剤として、塩素(Cl2)や二クロム酸塩(Cr2O72-)などがあり、それに次いで酸素(O2)がきます。これらは問題文の(エ)と(ア)です。
あまり強くないですが、3価の鉄(Fe3+)やヨウ素(I2)、2価の銅(Cu2+)なども一応、酸化剤として使われます。
残るのは(ウ)の水素イオン(H+)ですが、これはもう酸化剤と呼べるほどのものではありません。
以上から、上記の代表的な酸化剤を覚えて(イ)>(エ)>(ア)と並べ、そこにない(ウ)が最後にくる選択肢(4)が正解であると判断できます。

コメント