金属イオンを含む排水の処理に関する記述として、誤っているものはどれか。
- 金属イオンの水酸化物の溶解度積は、金属イオンの種類によって異なる。
- 3価の鉄イオンを含む酸性の排水にアルカリを加えていくと、水酸化物の沈殿を生じる。
- 製鉄所や金属表面処理工場からの酸洗い排水で2価の鉄イオンを含む場合、中和時に純窒素を吹き込んでFeを3価にしてから処理する。
- アルミニウム、鉛、亜鉛、クロムの水酸化物は両性水酸化物である。
- 両性水酸化物を作る金属の溶解度は、それぞれ特定のpH値において最低値を示す。
解 説
(1)は正しい記述です。また、金属の種類にも寄りますが、排水のpHの値によっても溶解度積が変わります。それを示したのが以下の図ですが、たまに同様の図を用いた出題もありますので、参考にしてください。
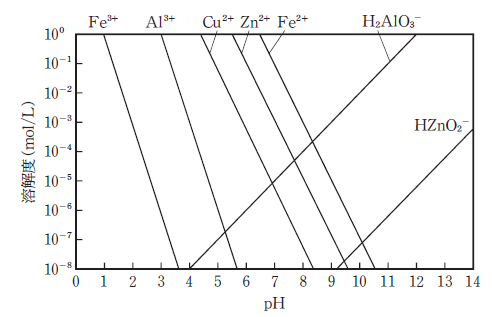
(2)も正しく、鉄に限らず多くの金属類は、pHがアルカリ側に傾くと水酸化物の沈殿を生じます。ただし、(4)や(5)にあるような両性金属は例外で、アルカリ側でも沈殿せず、水に溶けます。
(3)について、(1)の解説で使った表を見るとわかる通り、2価の鉄を処理しようとするとpHを10とか11くらいにしないと、ほぼ完全に沈殿除去することができません。それに対し3価の鉄であれば、pHを4程度にすればほぼ完全に沈殿除去できます。
一方、(3)の問題文にもあるように、製鉄所や金属表面処理工場からの「酸洗い」排水は、酸を使っているのでpHが低いです。もし鉄を2価のまま処理しようとすると、pHをぐっと上げるために大量のアルカリを使わなければならないので、先に3価の鉄に変えてから汚水処理を行います。2価の鉄を3価に変えるのは簡単で、汚水に空気を吹き込むことで空気中の酸素と反応(酸化)させるだけです。
(3)の記述のように「純窒素」を吹き込んでも反応しないので意味がなく、酸素が必要です。とはいえ、酸素ボンベなどをわざわざ用意する必要はなく、空気を吹き込めば充分なので、「純窒素」を「空気」に直せば正しい記述となります。
(4)について、両性金属といえば、アルミニウム、鉛、亜鉛、クロム、スズが挙げられます。よって、これは正しいです。
(5)で、多くの金属類は(1)の解説の図のように、極端にアルカリ側のpHにしてしまえば完全に沈殿します。しかし、両性金属は酸側でも水に溶け、アルカリ側でも水に溶けるので、その間に、最も溶けにくいちょうどよいpH値というのがあります。そのちょうどよいpH値は両性金属の種類ごとに異なるため、(5)の記述は正しいです。

コメント