問 題
嫌気処理において、グルコース(C6H12O6)が全量バイオガス(CH4とCO2の混合気体)になった場合、グルコース180gから生成する20℃でのバイオガス量(L)はいくらか。
ただし、20℃での気体のモル体積は24Lとする。また、原子量はH=1、C=12、O=16とする。
- 48
- 72
- 96
- 120
- 144
正解 (5)
解 説
グルコース(C6H12O6)が水(H2O)中で分解されてCH4とCO2に変わるという反応なので、その化学反応式は次のようになります。ただし、この段階では係数がよくわからないので、適当にa、b、cとしています。
![]()
ここで、反応前後でそれぞれの原子の数は変わらないので、各原子について比較して連立方程式を立てることで、係数a、b、cを求めることができます。
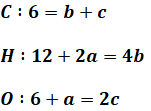
上の3式で連立方程式を解くと、a=0、b=3、c=3となるので、先ほど示した化学反応式は次のように書き換えることができます。
![]()
ここで、グルコース(C6H12O6)の分子量は12×6+1×12+16×6=180なので、180gでちょうど1molとなります。
上記の化学反応式より、1molのグルコースからはCH4とCO2がそれぞれ3molずつ、計6molできるため、生成するバイオガス量は次のように計算できます。
![]()

コメント