COとメタンの混合ガスを燃焼させたとき、最大CO2濃度が25%となるCOの割合は、およそ何%か。
- 40
- 50
- 60
- 70
- 80
正解 (5)
解 説
まず、COとメタンの燃焼の化学反応式は以下の通りです。
![]()
![]()
この問題ではCOの割合が問われているので、これを仮にaとします。すると、COの燃焼では、上式より、消費するO2はa/2で、生成するCO2はaになります。また、全体を1とするため、COがaなら、メタンは(1-a)で表すことができます。
メタンの燃焼では、上式より、消費するO2は2(1-a)で、生成するCO2は(1-a)となります。反応後に残るガスは、二酸化炭素と窒素(空気の酸素以外の成分)ですが、それらの量は以下の通りです(最大CO2濃度は乾き燃焼ガスにおいて考えるため、生成するH2Oについては無視します)。

ここで、窒素(空気の酸素以外の成分)の計算式について補足しておきます。
空気中には酸素が21%程度含まれていて、その他の成分が79%です(内訳は、窒素が約78%で、その他が約1%)。空気の成分のうち燃焼に関係するものは酸素だけなので、ここでは酸素21%と、窒素などは計79%としてまとめて考えます(以下、酸素以外の全ての成分を代表して「窒素」と表記します)。
窒素は燃焼反応に関わらないので、反応前に存在していた分が、反応後にもそのままの量で残っていることになります。その量の計算方法は上記の通りですが、空気全体を1とすると、窒素と酸素の比は0.79:0.21となることから、酸素の量に「0.79/0.21」を掛けることで、窒素量を計算することができます。
以上から、燃焼後のCO2濃度が25%になるようなaは、以下の計算式で求めることができます。
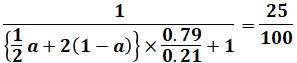
これを解くと、a=0.802となるので、答えは80%となります。

コメント