問 題
キレート剤を含む重金属排水の処理に関する記述として、誤っているものはどれか。
- キレート剤の存在量が多くなると、pH調整のみの単純な水酸化物法では重金属は処理できなくなる。
- キレート剤の濃度が低くなると錯体は不安定となる。
- キレート剤の影響は、キレート剤の種類、重金属の種類及び濃度により一様ではない。
- 置換法は、キレート剤で封鎖されている重金属を他の金属で置換し、置換された重金属を水酸化物として沈殿させる方法である。
- Fe+Ca塩法においては、重金属はまずCa2+によって置換され、その後Fe2+によって置換される。
正解 (5)
解 説
(1)は正しいです。キレート濃度が高いと金属イオンは錯体を形成するため、単なるpH調整では水酸化物として析出させにくくなっています。このような場合には、(4)の置換法や硫化物法などの処理が必要となります。
(2)も正しいです。錯体形成の平衡はキレート剤の濃度に依存するため、キレート剤の濃度が下がると錯体ができない方向(金属が遊離する方向)に平衡が傾きます。
(3)も正しいです。キレート剤と重金属の組合せや濃度によって、錯体形成のしやすさが変わります。そのため、主に処理したいと考えている重金属に合ったキレート剤を選ぶことが重要です。
(4)も正しいです。置換法は、キレート剤で封鎖されている重金属を他の無害な元素で置換し、置換された重金属を水酸化物として沈殿させる方法のことです。置換法にはMg塩法とFe+Ca塩法の二つがあります。
(5)が誤りです。Fe+Ca塩法は以下のような2段階の反応で構成されます(例として重金属を鉛Pbとしていますが、ほかの重金属でも同様です)。Fe+Ca塩法という名前の通り、1段階目でFeを、2段階目でCaを使っています。
- 1段階目(酸性条件)
![]()
- 2段階目(塩基性条件)
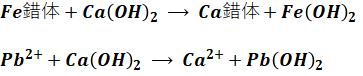
よって、(5)の記述は「Ca2+」と「Fe2+」が反対になっています。
以上から、正解は(5)です。

コメント