問 題
生物学的硝化脱窒素法における硝化槽(水理学的滞留時間8時間)に、アンモニア態窒素(NH4-N)濃度52mg/Lの排水が流入し、アンモニア態窒素(NH4-N)濃度10mg/Lで流出している。
単位容積(L)、単位時間(h)当たりに硝化のために消費される酸素量(mgO2/(L・h))として最も適切なものはどれか。
なお、流出水に亜硝酸は含まれないものとし、アンモニアの硝酸への酸化は次式で表されるものとする。

- 12
- 16
- 20
- 24
- 36
解 説
まずはアンモニア態窒素(NH4-N)の除去量について考えます。
NH4-Nの濃度は流入時に52[mg/L]で、流出時に10[mg/L]と書かれています。つまり、その差し引き52-10=42[mg/L]の分が硝化槽で除去されたことになります。
次に、単位時間あたりのNH4-Nの除去速度を求めます。
問題文より水理学的滞留時間(HRT)は8時間なので、単位時間あたりのNH4-N除去速度は次のように計算できます。

続いて、硝化反応における酸素消費量を計算します。
アンモニアの硝酸への酸化は、問題文で与えられている通り、下式のように表すことができます。

よって、1[mol]のNH4-Nを硝化するためには2[mol]のO2が必要です。また、NH4-Nの窒素分の原子量は14、消費するO2の分子量は32なので、1[mg]のNH4-Nを硝化するために必要なO2量は次のように算出できます。
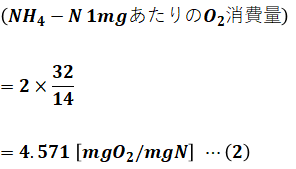
最後に、問われている「単位容積[L]、単位時間[h]あたりに硝化のために消費される酸素量[mgO2/(L・h)]を求めます。
上記の(1)式では、単位容積[L]、単位時間[h]あたりのNH4-Nの量がわかっていて、(2)式では、単位量のNH4-Nに対応するO2量がわかっています。そのため、求めたい消費酸素量[mgO2/(L・h)]は、これらの積で表すことができます。
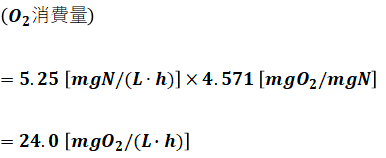
よって、正解は(4)となります。

コメント