問 題
次の文章は、鉛蓄電池に関する記述である。
鉛蓄電池は、正極と負極の両極に( ア )を用いる。希硫酸を電解液として初充電すると、正極に( イ )、負極に( ウ )ができる。これを放電すると、両極とももとの( ア )に戻る。
放電すると水ができ、電解液の濃度が下がり、両極間の電圧が低下する。そこで、充電により電圧を回復させる。過充電を行うと電解液中の水が電気分解して、正極から( エ )、負極から( オ )が発生する。
上記の記述中の空白箇所(ア)~(オ)に当てはまる組合せとして、正しいものを次の(1)~(5)のうちから一つ選べ。
- ア イ ウ エ オ
- 鉛 硫酸鉛 二酸化鉛 水素ガス 酸素ガス
- 鉛 二酸化鉛 硫酸鉛 酸素ガス 酸素ガス
- 硫酸鉛 鉛 二酸化鉛 水素ガス 酸素ガス
- 硫酸鉛 二酸化鉛 鉛 酸素ガス 水素ガス
- 二酸化鉛 硫酸鉛 鉛 酸素ガス 水素ガス
解 説
まず、鉛蓄電池の構成は以下の通りです。
鉛蓄電池:![]()
続いて、鉛蓄電池の充放電反応全体をまとめた化学反応式を以下に示します。
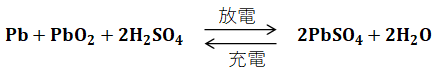
充電時の電極は正極が二酸化鉛(PbO2)、負極が鉛(Pb)ですが、放電後にはどちらも硫酸鉛(PbSO4)となります。つまり、上記の左側から右側への反応が放電で、反対に右側から左側への反応が充電です。
上記の化学反応式は鉛蓄電池の反応全体をまとめたものですが、それぞれの電極では次のような反応が起こっています。放電時または充電時の片方を覚えてしまえば、他方はその逆になっているだけです。
(放電・正極) ![]()
(放電・負極) ![]()
(充電・正極) ![]()
(充電・負極) ![]()
以上を踏まえて問題文を見ると、( ア )は充電前の正極・負極なので「硫酸鉛」で、( イ )は充電後の正極なので「二酸化鉛」、( ウ )は充電後の負極なので「鉛」となります。
よって、選択肢から(4)が正解だと決まります。鉛蓄電池に関しては上記までが重要なので、ここまでをしっかり覚えておけば、( エ )と( オ )がわからなくても正解できるような選択肢になっています。
( エ )と( オ )は水の電気分解がテーマです。水(H2O)を電気分解すると、次に示す化学反応式によって、水素ガス(H2)と酸素ガス(O2)が生成します。
![]()
この際、正極に酸素ガス(O2)、負極に水素ガス(H2)が発生するので、( エ )は「酸素ガス」、( オ )は「水素ガス」となります。
この反応についても上記の鉛蓄電池で示したのと同じように正極・負極ごとのイオン式で示すことができますが、出題頻度から考えて、そのまま結論を覚えてしまったほうが早いと思います。
以上から、
- ( ア ):硫酸鉛
- ( イ ):二酸化鉛
- ( ウ ):鉛
- ( エ ):酸素ガス
- ( オ ):水素ガス
となるので、正解は(4)です。

コメント